- Obtener vínculo
- X
- Correo electrónico
- Otras apps
- Obtener vínculo
- X
- Correo electrónico
- Otras apps
Ejercicios
resueltos de oxidos básicos:

a)
Fe2O3
b)
CO
c)
SO3
d)
CuO
e)
NO2
f)
Na2O
g)
MgO
Solución:
Comenzaremos
diciendo que el óxido se forma con la combinación quimica del
oxígeno con otro elemento químico:
Oxígeno + Elemento Químico → Óxido
Existen
dos tipos de óxidos:
- Óxidos básicos: Combinación química del oxígeno con un metal
- Óxidos ácidos: Combinación química del oxígeno con un no metal
Hasta
el momento hemos repasado la teoría y vemos que no es nada del otro
mundo. Vayamos al ejercicio y definamos si cada uno de los elementos
que acompañan al oxígeno es metal o no metal.
a)
Fe2O3:
El elemento que acompaña al oxígeno es el hierro (Fe), es un metal.
Por lo tanto es un óxido
básico.
Oxígeno + Elemento Metálico → Óxido Básico
b)
CO : El elemento que acompaña al oxígeno es el carbono (C), es un
no metal. Por lo tanto es un óxido
ácido.
Oxígeno + Elemento No Metálico → Óxido Ácido
Igualmente
para los demás:
c)
SO3:
El azufre (S) es un no metal, entonces es un óxido ácido
d)
CuO: El cobre (Cu) es un metal, entonces es un óxido básico
e)
NO2:
El nitrógeno (N), es un no metal, entonces es un óxido ácido
f)
Na2O
: El sodio (Na) es un metal, entonces es un óxido básico
g)
MgO : El magnesio (Mg) es un metal, entonces es un óxido básico
Ejercicio 2:
Se
disponen de los siguientes óxidos básicos: Na2O
, BaO , Li2O
, PbO2
¿Qué
nombres están bien formulados según la nomenclatura tradicional?
a)
Na2O : óxido sódico
b)
BaO : óxido barioso
c)
Li2O : monóxido litoso
d)
PbO2: óxido plúmbico
Solución:
Para
nombrar un óxido básico (óxido metálico), según la nomenclatura
tradicional se
emplean sufijos de acuerdo al numero de oxidación del metal.
Usaremos la siguiente tabla:

Comencemos¡¡
a)
Na2O
:El
sodio (Na) tiene valencia única
Valencia (Na) : 1
Según
la tabla anterior, corresponde al caso de valencia única (fila 1)
Su
nomenclatura sería: Óxido sódico
b)
BaO :El
bario (Ba) tiene valencia única
Valencia (Ba) : 2
De
la tabla correspondería al caso de valencia única (fila 1)
Su
nomenclatura sería: Óxido bárico
c)
Li2O
:El
litio (Li) tiene valencia única
Valencia (Li) : 1
Según
la tabla anterior, corresponde al caso de valencia única (fila 1)
Su
nomenclatura sería: Óxido lítico
d)
PbO2:
El plomo (Pb) tiene dos valencias
Valencia (Pb) : 2 , 4
Sabemos
que la formulación general del óxido es:
- Para valencia (Pb) : 2 → Pb2O2 → PbO
- Para valencia (Pb) : 4 → Pb2O4 → PbO2
En
nuestro caso correspondería al plomo con valencia = 4 (mayor
valencia)
De
la tabla correspondería al caso con 2 valencias (valencia mayor,
fila 3)
Su
nomenclatura sería: Óxido plúmbico
Ahora
se puede verificar que las alternativas que están bien formuladas
son “a” y “d”.
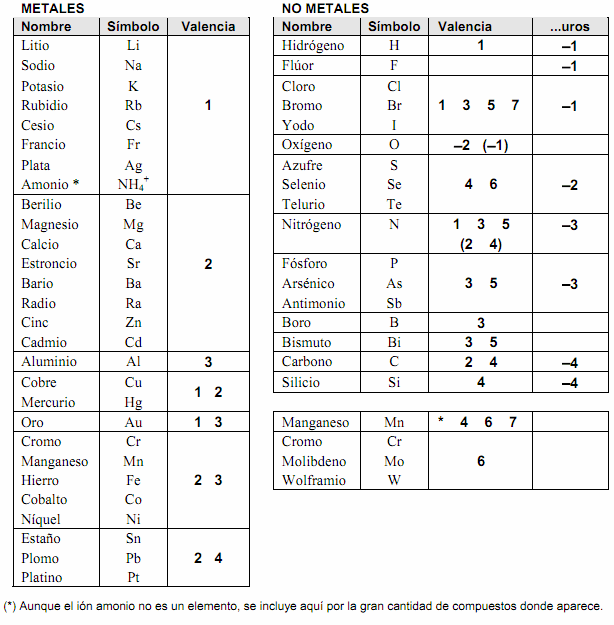
Si
desea ver la tabla de valencias acá les dejo una imagen:

Comentarios
Publicar un comentario